Диффузионное и кинетическое горение
В основе процесса горения, происходящего в атмосфере воздуха, лежит химическая реакция между горючим веществом и кислородом. Скорость горения вещества, по-видимому, должна целиком зависеть от скорости химической реакции. Однако это часто бывает не так. Рассмотрим следующий опыт. В газовую горелку, представляющую собой металлическую трубку, подадим с небольшой скоростью горючий газ метан (СН4). Если к срезу горелки поднести источник зажигания, то газ воспламенится и над срезом горелки установится пламя (рис. 1.2).
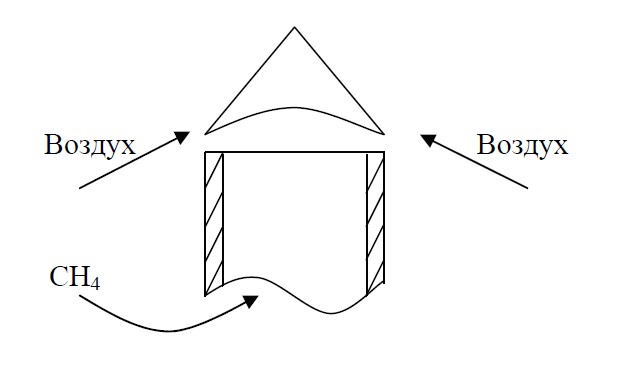
Рис. 1.2. Диффузионное горение метана
Рассмотрим подробнее как в этом случае происходит процесс горения. Чтобы произошла химическая реакция между горючим и окислителем. кислород из воздуха, а метан из трубки должны продиффундировать в зону горения и образовать там горючую смесь. И только потом между ними происходит химическая реакция. В этом опыте процесс горения складывается из двух следующих друг за другом процессов: диффузии и химической реакции. Причем скорость диффузии молекул метана и кислорода в зону горения значительно ниже, чем скорость, с которой они вступают в химическую реакцию. Формально скорость горения будет равна
\(U_{гор}= {\bigtriangleup m_ {CH_4} \over \tau _д+ \tau _{х р}}\)
где
ΔmCH4 - количество продиффундировавшего и прореагировавшего метана за время (тд+тхр):
тд+тхр - время диффузии и время химической реакции.
Так как
тд ≪ тхр
\(U_{гор}= {\bigtriangleup m_ {CH_4} \over \tau _д}\)
Отношение ΔmCH4/ тд по сути дела есть скорость диффузии, а это означает. что скорость горения в этом опыте определяется скоростью диффузии. т. е. скоростью смесеобразования.
Такое горение называют диффузионным.
При таком горении зона горения размыта, пламя имеет желтый оттенок. Из-за наличия в зоне химических реакций областей с низким содержанием окислителя в процессе горения образуются продукты неполного окисления, пламя коптит.
Теперь представим другой опыт. В эту же горелку подадим не один метан, а смесь метана с воздухом (рис. 1.3).
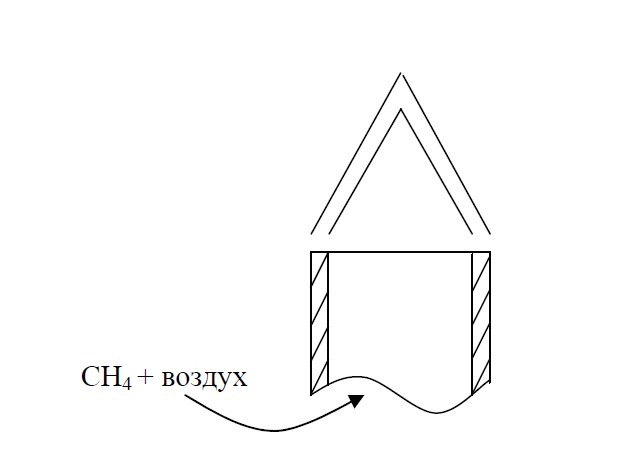
Рис. 1.3. Кинетическое горение метана
В зону химических реакций будет попадать уже готовая к горению горючая смесь. Это означает, что тД= 0. смесеобразование происходит как бы мгновенно. Тогда из формулы (1.12) следует:
\(U_{гор}= {\bigtriangleup m_ {CH_4} \over \ \tau _{х р}}\)
где
Величина ΔmCH4/ тхр пропорциональна скорости химической реакции, поэтому скорость горения в этом случае зависит только от скорости химической реакции, которая значительно выше скорости диффузии.
Экспериментально это сразу будет заметно, в таком опыте придется увеличить скорость подачи газа, иначе пламя резко опустится и уйдет в трубку. Зона горения в этом опыте резко очерчена, пламя имеет голубой цвет.
Такое горение называется кинетическим.
Кинетическое горение газа можно наблюдать на горелках кухонной газовой плиты. Горелки устроены так. что в них при прохождении газа подсасывается воздух и в зону горения попадает уже газовоздушная смесь.
Кинетическому горению свойственно более полное сгорание, более высокая скорость горения и. как следствие, высокая скорость тепловыделения (Дж/с) и высокая температура пламени.
При кинетическом горении зона горения, т. е. зона химических реакций. представляет собой четко выраженную светящуюся область определенной толщины, называемую фронтом пламени, который отделяет свежую горючую смесь от продуктов горения.
На газовой горелке фронт пламени кажется неподвижным, так как его положение не меняется во времени относительно самой горелки. Однако на самом деле он движется по горючей газовой смеси со скоростью, равной скорости движения этой смеси относительно горелки. В этом можно легко убедиться, если уменьшить или прекратить подачу горючей газовой смеси, пламя в этом случае уйдет в горелку до места смешения горючего и окислителя.
Итак, если смесь горючего и окислителя заранее перемешана, то по такой смеси пламя может перемешаться. Возникнув в одной какой-то точке пространства, горение будет распространяться во все стороны на всю горючую газовую смесь.
Самопроизвольное распространение пламени - одно из основных отличительных свойств процесса горения. Кинетическое горение, т. е. распространение пламени по газовой горючей смеси, как правило, наблюдается на стадии возникновения пожара газов и горючих жидкостей. В результате утечки газа или испарения горючей жидкости в воздухе может образоваться паровоздушная смесь, способная распространять пламя. Если в зоне опасных концентраций горючего появится источник зажигания, то около него возникнет горение и пламя начнет распространяться по всей горючей газовоздушной смеси.
Пример диффузионного и кинетического горения можно посмотреть на видео:
Дефлаграционное и детонационное горение
Скорость распространения фронта пламени по газовоздушным смесям может изменяться в пределах от 0.5 до 50 м/с в зависимости от горючего вещества. Скорость распространения пламени зависит не только от скорости химической реакции между горючим и окислителем, но и от скорости передачи тепла от зоны горения в холодную свежую смесь, так как процесс горения представляет собой непрерывное последовательное воспламенение и сгорание все новых и новых порций горючей смеси.
Распространение пламени со скоростью движения тепловой волны называется нормальным или дефлаграционным.
При определенных условиях в некоторых горючих смесях, таких, как Н2+О2 (гремучая смесь). С2Н2+О2, С3Н6+О2 и др., может возникнуть совершенно другой режим распространения пламени, когда пламя распространяется не по механизму теплопроводности, а по механизму ударной волны - волны сжатия. В этом случае скорость распространения пламени превышает скорость звука и достигает значений от нескольких сот метров до нескольких километров в секунду. Такое горение называют взрывным или детонационным.
Таким образом, по механизму распространения пламени и соответственно по скорости распространения пламени различают дефлаграционное и детонационное горение.
Дефлаграционному (нормальному) горению свойственны скорости распространения пламени 0.5—50 м/с, а детонационному (взрывному) горению 500-3000 м/с.
Детонационное горение обладает большой разрушительной силой. Однако встречается этот вид горения достаточно редко. Для возникновения детонационного горения даже в системах, склонных к детонации необходимы специальные условия. Детонация, как правило, возникает в закрытых объемах и длинных трубах, когда создаются условия для ускорения пламени.
Пример детонационного горения Вы можете просмотреть на видео.
Гомогенное и гетерогенное горение
Во всех рассмотренных примерах горение происходило в газовой фазе. горючее и окислитель в зоне горения находились в одинаковом состоянии - газообразном. Такое горение, при котором оба компонента (горючее и окислитель) в зоне химических реакций находятся в одинаковой фазе (агрегатном состоянии), называют гомогенным или однофазным. Если же в зоне горения горючее и окислитель находятся в разных фазах, горение называют гетерогенным (разнофазным).
Гомогенным горением является не только горение газов, но и горение жидкостей, а также большинства твердых горючих материалов. Объясняется это тем. что при горении жидкостей горит не сама жидкость, а ее пары. В результате испарения с поверхности жидкости непрерывно в газовую фазу поступают пары горючего вещества, которые, смешиваясь с окружающим воздухом, образуют горючую паровоздушную смесь. Именно здесь в паровоздушной смеси, а не на поверхности жидкости будут происходить химические реакции горения. Визуально можно наблюдать, что пламя (зона горения) как бы немного оторвано от поверхности жидкости.
Похожая картина наблюдается и при горении большинства твердых горючих материалов: парафина, оргстекла, полиэтилена, древесины, торфа. хлопка, резины, различных пластмасс. На их поверхности под воздействием тепловых потоков могут происходить различные физико-химические процессы (плавление, испарение, термическое разложение). В результате образуются газообразные горючие вещества, которые и вступают в химическую реакцию горения с кислородом воздуха. Таким образом, и в случае твердых горючих материалов горючее вещество и окислитель в зоне горения оказываются в одной фазе, в одном агрегатном состоянии. Поскольку химические реакции горения происходят в газовой фазе, то над поверхностью твердого горючего материала наблюдается пламя. Наличие пламени является отличительным признаком гомогенного горения.
Примером гетерогенного горения может служить горение углерода (графит или углистый остаток после термического разложения древесины), который даже при высоких температурах остается в твердом состоянии. Кислород воздуха диффундирует к твердой поверхности и при достаточно высокой температуре (700-800 °C) на поверхности будет происходить химическая реакция между твердым углеродом и газообразным кислородом. Пламя в этом случае отсутствует, а признаком гетерогенного горения углерода будет являться ярко красное свечение поверхности углерода. Такое горение называется тлением. Некоторые твердые горючие материалы, способные к гомогенному горению, такие, как древесина, бумага, хлопок и др., могут тлеть в случае, если количество теплоты, поступающее к поверхности этого материала, мало для обеспечения интенсивного термического разложения материала с образованием газообразных горючих веществ. При гетерогенном горении существует поверхность раздела фаз (твердой и газовой), именно на поверхности раздела фаз и происходят химические реакции. Гетерогенное горение является диффузионным, так как прежде чем произойдет химическая реакция между горючим и окислителем необходимо, чтобы кислород продиффундировал к поверхности раздела фаз. которая в данном случае и является зоной горения.
Гомогенное горение бывает как диффузионным, так и кинетическим. Если имеется готовая горючая газовая смесь, т. е. горючее и окислитель в ней заранее перемешаны, то в ней будет наблюдаться кинетическое горение. при котором пламя распространяется по горючей смеси. Если же смешение горючего и окислителя происходит непосредственно в зоне горения, как это имеет место при истечении горючего газа в окислительную среду, то горение будет диффузионным. Из этого можно сделать вывод, что горение жидкостей и большинства твердых горючих материалов является гомогенным и диффузионным. Диффузионное пламя будет располагаться там. где при смешении образуется горючая газовая смесь.
Ламинарное и турбулентное горение
Гомогенное, диффузионное горение образовано потоком горючего газа, втекающим в окислительную среду. В зависимости от скорости потока. его диаметра и вязкости среды движение может быть ламинарным или турбулентным. Также и возникающее диффузионное пламя может быть ламинарным или турбулентным. Ламинарное пламя образуется при низких скоростях потока горючего и небольшом его диаметре. Ламинарное горение воспринимается как спокойное горение, когда пламя неподвижно относительно окружающей среды. Такое пламя можно наблюдать при горении свечи, при горении газа в горелке, если скорость истечения небольшая, а также при горении жидкости в небольших тиглях.
С увеличением скорости и диаметра потока газообразного горючего вещества происходит его турбулизация, появляются завихрения, пламя становится неустойчивым. Турбулизация пламени приводит к увеличению скорости смесеобразования и. как следствие, к увеличению скорости горения.
Развитый турбулентный режим горения наблюдается на пожарах газовых фонтанов, крупных резервуаров с горючими жидкостями, больших штабелей древесины.
Ламинарный и турбулентный режимы горения характерны как для диффузионного, так и для кинетического пламени. При ламинарном кинетическом горении фронт пламени гладкий, движение его спокойное. При турбулизации кинетического горения происходит искривление фронта, образуются вихри и фронт разбивается на отдельные очаги. При этом скорость горения увеличивается, увеличивается и скорость движения зоны горения. Турбулизации кинетического горения и его ускорению способствует наличие препятствий на пути движения фронта. Так. кинети-ческое пламя хорошо турбулизуется и ускоряется в загроможденных помещениях. Турбулизация и ускорение китентического пламени может способствовать переходы дефлаграционного горения в детонацию.
Пример турбулентного горения в видео:
